
Goutte et hyperuricémie en 2026 : de la physiopathologie aux nouvelles thérapies
aiguës. En 2026, cette pathologie complexe, intimement liée à l’hyperuricémie et au risque cardiovasculaire, connaît une évolution majeure tant dans sa compréhension que dans sa prise en charge. Loin de se résumer à la classique crise du gros orteil, la goutte est désormais reconnue comme une maladie systémique nécessitant une approche globale. Cet article fait le point sur les données épidémiologiques récentes, les mécanismes physiopathologiques sous-jacents et les avancées thérapeutiques prometteuses, notamment celles présentées lors des derniers congrès internationaux.
-
La prévalence de la goutte a augmenté de plus de 20 % au cours des trente dernières années, touchant des dizaines de millions de personnes dans le monde.
-
L’hyperuricémie chronique, définie sur le plan physiopathologique par un taux d’acide urique supérieur à son seuil de solubilité (environ 68 mg/L ou 400 µmol/L), est le facteur déclenchant principal par la formation de cristaux d’urate monosodique.
-
La goutte est fortement associée au syndrome métabolique et à un sur-risque cardiovasculaire et rénal.
-
Les recommandations actuelles (EULAR/ACR) insistent sur un traitement hypo-uricémiant ciblé (uricémie < 60 mg/L, voire < 50 mg/L en cas de tophus), particulièrement indiqué en cas de crises fréquentes, de tophi ou de lésions structurales.
-
De nouvelles thérapies expérimentales, telles que le firsekibart (un anti-IL-1β), et l’utilisation d’inhibiteurs SGLT2 en cas de comorbidités, ouvrent des perspectives inédites pour les patients complexes.
Une épidémiologie en constante évolution
La goutte n’est plus une maladie rare. Les données épidémiologiques mondiales récentes mettent en évidence une augmentation constante de son incidence et de sa prévalence. Cette tendance s’explique par le vieillissement de la population, mais surtout par l’évolution des modes de vie et l’explosion des maladies métaboliques.
Un fardeau mondial croissant
Selon les analyses épidémiologiques récentes, la prévalence de la goutte a connu une augmentation de plus de 20 % sur les trois dernières décennies, touchant aujourd’hui des dizaines de millions de personnes à travers le monde [1]. Les projections suggèrent que ce fardeau continuera de s’alourdir dans les décennies à venir, en lien avec le vieillissement démographique et les facteurs métaboliques [1].
Cette augmentation n’est pas uniforme à l’échelle mondiale. Les pays à hauts revenus, comme les États-Unis, l’Australie et le Canada, ont enregistré de fortes hausses de prévalence [1]. Cependant, on observe également un déplacement progressif du fardeau de la maladie vers les pays à revenus faibles et intermédiaires [1].
Le profil type du patient goutteux
La goutte reste une pathologie à prédominance masculine. La prévalence est environ trois fois plus élevée chez les hommes que chez les femmes [1]. Cette différence s’explique en grande partie par l’effet uricosurique (qui favorise l’élimination de l’acide urique par les reins) des œstrogènes, protégeant ainsi les femmes jusqu’à la ménopause [2].
L’âge est un facteur de risque majeur. La maladie se développe généralement à l’âge moyen chez l’homme et après la ménopause chez la femme [2]. Chez les personnes de 65 ans et plus, la prévalence standardisée est particulièrement élevée [1]. La goutte à début précoce (avant 30 ou 40 ans) reste rare et doit faire rechercher une composante héréditaire forte ou un déficit enzymatique spécifique [2].
De l’hyperuricémie à la crise de goutte : comprendre la physiopathologie
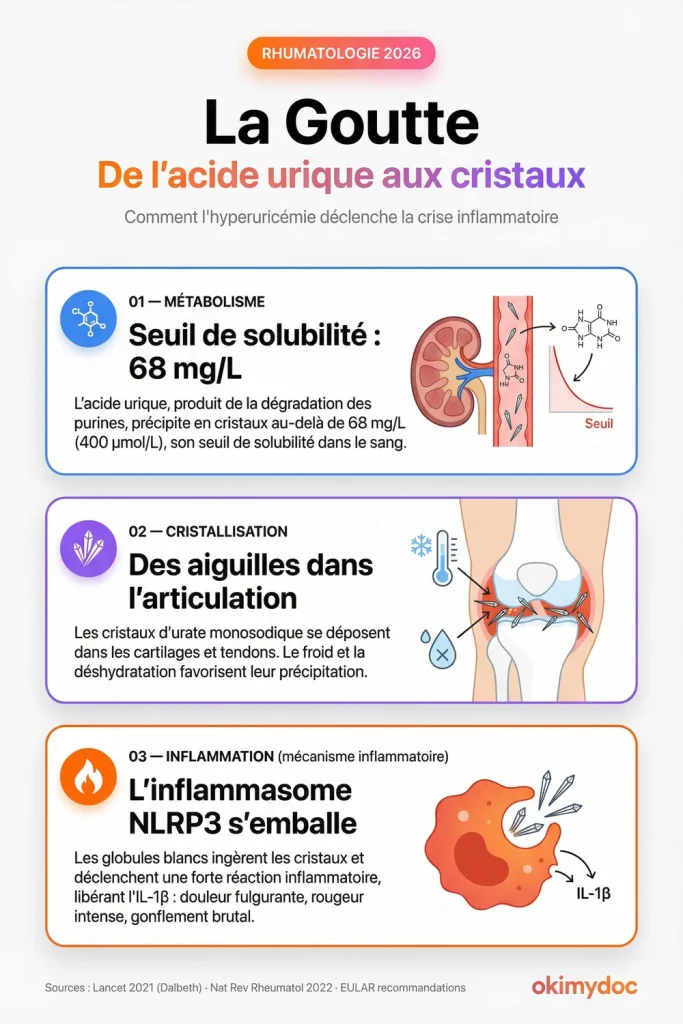
Pour comprendre la goutte, il faut d’abord s’intéresser à l’acide urique, une molécule au cœur du processus pathologique. La goutte est la conséquence clinique directe d’une hyperuricémie chronique, bien que toutes les hyperuricémies ne conduisent pas nécessairement à la goutte.
Le métabolisme de l’acide urique et définition de l’hyperuricémie
L’acide urique est le produit final de la dégradation des purines chez l’être humain [3]. Les purines proviennent de deux sources : la dégradation des cellules de notre propre organisme (turnover cellulaire) et notre alimentation (viandes, abats, crustacés) [3]. La transformation finale en acide urique est catalysée par une enzyme clé : la xanthine oxydase [3].
Contrairement à la plupart des mammifères, l’être humain a perdu au cours de l’évolution l’enzyme uricase, capable de dégrader l’acide urique en allantoïne, une substance beaucoup plus soluble [3]. Par conséquent, l’acide urique humain est peu soluble dans le sang et les fluides corporels.
Sur le plan physiopathologique, l’hyperuricémie est définie par un taux d’acide urique sérique supérieur à son seuil de solubilité, qui se situe aux alentours de 68 mg/L (400 µmol/L) à température corporelle normale [2] [4]. Au-delà de ce seuil, le risque de précipitation sous forme de cristaux augmente considérablement. Les valeurs souvent citées de 60 mg/L ou 50 mg/L ne définissent pas l’hyperuricémie en soi, mais correspondent aux objectifs thérapeutiques fixés pour dissoudre les cristaux [4].
Les causes de l’hyperuricémie
L’hyperuricémie résulte d’un déséquilibre entre la production et l’élimination de l’acide urique. Dans plus de 90 % des cas, elle est due à un défaut d’excrétion rénale [2].
-
Défaut d’excrétion rénale : C’est la cause la plus fréquente. Elle peut être d’origine génétique, liée à une insuffisance rénale, ou induite par certains médicaments (diurétiques thiazidiques et de l’anse, aspirine à faible dose, ciclosporine) [2].
-
Surproduction d’acide urique : Plus rare, elle s’observe lors d’un renouvellement cellulaire accéléré (hémopathies, psoriasis étendu, traitements cytotoxiques) ou en cas de déficits enzymatiques héréditaires [2].
-
Facteurs alimentaires : Une alimentation riche en purines, la consommation d’alcool (particulièrement la bière, riche en purines, et les spiritueux) et les boissons sucrées au fructose (sodas, jus de fruits) augmentent la production d’acide urique et diminuent son excrétion [3].
La formation des cristaux et l’inflammation
Lorsque l’hyperuricémie se prolonge, l’acide urique précipite sous forme de cristaux d’urate monosodique (UMS) [2]. Ces cristaux en forme d’aiguilles se déposent préférentiellement dans les tissus peu vascularisés, comme le cartilage articulaire, les tendons et les bourses séreuses [2]. La cristallisation est favorisée par des facteurs locaux tels que le froid (ce qui explique l’atteinte fréquente des extrémités comme le gros orteil), la déshydratation ou une acidose locale [3].
La crise de goutte aiguë est déclenchée lorsque ces cristaux sont libérés dans l’espace articulaire et phagocytés (ingérés) par les cellules immunitaires, notamment les macrophages [2]. Ce processus active un complexe protéique intracellulaire appelé inflammasome NLRP3, qui déclenche la production massive d’interleukine-1 bêta (IL-1β), une cytokine fortement pro-inflammatoire [4]. C’est cette cascade inflammatoire qui provoque la douleur fulgurante, la rougeur et le gonflement caractéristiques de la crise.
Les tophi et l’atteinte systémique
Avec le temps et en l’absence de traitement de fond, les dépôts de cristaux s’accumulent et forment des tophi (ou tophus au singulier) [2]. Ces nodules sous-cutanés, parfois visibles et palpables, se localisent souvent sur le pavillon de l’oreille, les coudes (bursite olécrânienne), les doigts ou le tendon d’Achille [2]. Ils peuvent causer des destructions articulaires irréversibles (arthropathie uratique) [2].
Au-delà de l’articulation, la goutte est fortement associée au syndrome métabolique (, diabète de type 2, , obésité) et à un sur-risque cardiovasculaire et rénal [5]. La présence de cristaux d’urate et l’inflammation chronique de bas grade qui en découle pourraient contribuer à la dysfonction endothéliale et à l’athérosclérose, justifiant une prise en charge globale du patient [5].
Diagnostic et prise en charge en 2026 : les recommandations actuelles
Le diagnostic de la goutte repose sur un faisceau d’arguments cliniques, biologiques et radiologiques. La prise en charge a considérablement évolué, passant d’un simple traitement symptomatique des crises à une stratégie proactive de contrôle de l’uricémie (« treat-to-target »).
Un diagnostic de plus en plus précis
La présentation clinique classique est la monoarthrite aiguë du gros orteil (podagre), survenant souvent la nuit, avec une douleur insupportable, une rougeur et un gonflement [2]. Cependant, d’autres articulations peuvent être touchées (cheville, genou, poignet).
Le diagnostic de certitude (le « gold standard ») reste la mise en évidence de cristaux d’urate monosodique dans le liquide synovial prélevé par ponction articulaire [2]. Ces cristaux apparaissent en forme d’aiguilles et sont fortement biréfringents en lumière polarisée [2].
L’imagerie joue un rôle grandissant. Les recommandations EULAR (European Alliance of Associations for Rheumatology) soulignent l’importance de l’échographie articulaire et du scanner à double énergie (DECT) [6]. L’échographie peut révéler le signe du « double contour » (dépôt de cristaux sur le cartilage) ou des tophi infracliniques [6]. Le DECT permet de visualiser et de quantifier spécifiquement les dépôts d’acide urique dans l’ensemble du corps [6].
Le bilan biologique initial doit inclure le dosage de l’uricémie, mais aussi l’évaluation de la fonction rénale (débit de filtration glomérulaire) et la recherche de facteurs de risque cardiovasculaire (glycémie, bilan lipidique) [7].

Traitement de la crise aiguë : agir vite
L’objectif lors d’une crise est de soulager la douleur et l’inflammation le plus rapidement possible, idéalement dans les 12 premières heures [7]. Les options thérapeutiques de première ligne recommandées par l’ACR (American College of Rheumatology) et l’EULAR comprennent :
-
La colchicine : Efficace si administrée tôt. Les doses recommandées ont été revues à la baisse pour limiter la toxicité (ex: 1 mg d’emblée, puis 0,5 mg une heure plus tard) [7].
-
Les : Comme le naproxène, à pleine dose sur une courte période, en l’absence de contre-indications (insuffisance rénale, ulcère, risque cardiovasculaire) [7].
-
Les corticoïdes : Par voie orale (prednisone) ou en infiltration intra-articulaire, particulièrement utiles en cas de contre-indication aux AINS ou à la colchicine [7].
Le repos de l’articulation et l’application de glace sont des mesures adjuvantes importantes [7].
Le traitement de fond : la stratégie « Treat-to-Target »
Le véritable enjeu de la prise en charge de la goutte est le traitement de fond hypo-uricémiant (THU). Son but est de dissoudre les cristaux existants et de prévenir la formation de nouveaux dépôts en maintenant l’uricémie en dessous du seuil de saturation.
Les recommandations internationales (ACR 2020, EULAR) préconisent d’initier un THU particulièrement chez les patients présentant des tophi, des lésions structurales radiographiques, ou des crises fréquentes (au moins deux par an) [7].
La cible thérapeutique (stratégie « treat-to-target ») est stricte :
-
Uricémie < 60 mg/L (360 µmol/L) pour la majorité des patients traités [7].
-
Uricémie < 50 mg/L (300 µmol/L) pour les patients souffrant de goutte sévère (tophi, arthropathie) afin d’accélérer la dissolution des dépôts [7].
Les médicaments hypo-uricémiants de première intention sont les inhibiteurs de la xanthine oxydase :
-
L’allopurinol : Le traitement de référence. Il doit être initié à faible dose (≤ 100 mg/jour, voire moins en cas d’insuffisance rénale) et augmenté progressivement (titration) jusqu’à l’atteinte de la cible [7]. Cette précaution est cruciale pour éviter les toxidermies graves (syndrome de DRESS, syndrome de Stevens-Johnson) [7].
-
Le fébuxostat : Une alternative efficace, souvent utilisée en cas d’intolérance ou d’échec de l’allopurinol [7].
Lors de l’initiation du THU, la baisse rapide de l’uricémie peut paradoxalement déclencher des crises de goutte par mobilisation des cristaux. Une prophylaxie par colchicine à faible dose (0,5 à 1 mg/jour) ou par AINS est donc fortement recommandée pendant les 3 à 6 premiers mois du traitement [7].

Mesures hygiéno-diététiques et gestion des comorbidités
Le traitement médicamenteux doit s’accompagner de modifications du mode de vie [7] :
-
Perte de poids progressive en cas de surpoids.
-
Arrêt de la consommation de bière (même sans alcool) et d’alcools forts.
-
Limitation des sodas et jus de fruits riches en fructose.
-
Réduction de la consommation de viandes rouges, d’abats et de crustacés.
-
Encouragement de la consommation de produits laitiers allégés (effet uricosurique) et d’une bonne hydratation.
La révision des traitements en cours est également essentielle. Si possible, les diurétiques hyperuricémiants doivent être remplacés par des antihypertenseurs ayant un effet uricosurique, comme le losartan ou l’amlodipine [7].
Les espoirs de la recherche : nouvelles thérapies et approches en 2026
Malgré l’existence de traitements efficaces, une proportion de patients reste en échec thérapeutique (goutte réfractaire) ou présente des contre-indications aux traitements standards. La recherche s’est donc intensifiée pour proposer de nouvelles options.
Le firsekibart : un traitement expérimental prometteur
Le firsekibart est un nouvel anticorps monoclonal entièrement humain dirigé contre l’interleukine-1 bêta (IL-1β), actuellement en phase de développement clinique [8]. Lors de récents congrès de rhumatologie, les résultats d’essais de phase III évaluant cet anti-IL-1β dans la crise de goutte aiguë ont été présentés [8].
L’étude a inclus des patients souffrant d’arthrite goutteuse aiguë pour lesquels les options thérapeutiques classiques étaient limitées. Le firsekibart a démontré une efficacité supérieure sur la douleur par rapport au traitement de contrôle [8]. Bien qu’il s’agisse encore d’un traitement expérimental, ces résultats confirment l’intérêt de cibler la voie inflammatoire de l’IL-1β, impliquée dans la crise de goutte, chez les patients en impasse thérapeutique.
Les inhibiteurs SGLT2 : un intérêt en cas de comorbidités
Les inhibiteurs du cotransporteur sodium-glucose de type 2 (SGLT2), ou gliflozines, sont des médicaments bien établis pour le traitement du diabète de type 2, de l’insuffisance cardiaque et de la maladie rénale chronique. Récemment, des études ont mis en évidence que ces molécules favorisent également l’excrétion urinaire de l’acide urique, entraînant une baisse modérée de l’uricémie [9].
Bien que les inhibiteurs SGLT2 ne soient pas un traitement spécifique de la goutte, leur utilisation est associée à une réduction du risque de crises de goutte dans certaines études, notamment chez les patients diabétiques [9]. Sachant que la goutte est fortement associée au syndrome métabolique, ces molécules représentent une option particulièrement intéressante pour la prise en charge globale des patients goutteux présentant des comorbidités cardio-rénales ou un diabète, en complément du traitement hypo-uricémiant standard [9].
Conclusion
En 2026, la goutte ne doit plus être considérée comme une fatalité douloureuse. La compréhension fine de sa physiopathologie, l’amélioration des techniques d’imagerie et l’évolution des recommandations vers une stratégie de traitement ciblée (« treat-to-target ») permettent aujourd’hui une prise en charge optimale. L’arrivée de nouvelles thérapies expérimentales ciblées offre des perspectives encourageantes pour les patients les plus sévèrement atteints. Le défi majeur reste l’éducation thérapeutique : faire comprendre que la goutte est une maladie chronique nécessitant un traitement de fond au long cours, bien au-delà de la simple gestion des crises aiguës, et une prise en charge globale du risque cardiovasculaire associé.
Références
[1] Tang X, et al. Global, regional, and national burden of gout among older adults: epidemiological modeling from 1990 to 2021 with projections to 2050. Front Med. 2025.
[2] Dalbeth N, et al. Gout. Lancet. 2021;397(10287):1843-1855.
[3] Punzi L, et al. Gout: one year in review 2025. Clin Exp Rheumatol. 2025;43:799-808.
[4] Stamp LK, Dalbeth N. Critical appraisal of serum urate targets in the management of gout. Nat Rev Rheumatol. 2022;18:403-412.
[5] Association of hyperuricemia with coronary heart disease and other cardiovascular outcomes: A systematic review and dose-response meta-analysis. PLoS One. 2025.
[6] Mandl P, et al. 2023 EULAR recommendations on imaging in diagnosis and management of crystal-induced arthropathies in clinical practice. Ann Rheum Dis. 2024;83(6):752-760.
[7] FitzGerald JD, et al. 2020 American College of Rheumatology Guideline for the Management of Gout. Arthritis Care Res (Hoboken). 2020;72(6):744-760.
[8] Xue Y, et al. Firsekibart versus compound betamethasone in acute gout: a phase 3 trial. Ann Rheum Dis / ACR Convergence. 2025.
[9] Doménech-Serrano J, et al. Combination of sodium-glucose cotransporter type 2 inhibitors and urate-lowering therapy in gout. Front Med. 2025.
Article rédigé par le Dr Michel Bensadoun, L’auteur ne déclare aucun conflit d’intérêts concernant cet article.
Note : Cet article a été rédigé avec l’aide de l’intelligence artificielle, notamment pour l’assistance à la rédaction et à l’illustration. Le contenu a été soigneusement relu, validé et complété par l’auteur pour garantir sa fiabilité et sa pertinence.
Important : Cet article n’a pas vocation à remplacer une consultation médicale. Chaque situation est unique et nécessite une prise en charge individualisée.


Leave a Comment